Vous êtes ici : UVSQ RechercheActualités de la recherche | Innovation
- Mis à jour le 2 mai 2023
- Version PDF
De nouveaux résultats pour contrer le virus respiratoire syncytial
Les résultats d'une étude autour du blocage de la multiplication du virus respiratoire syncytial, responsable de la bronchiolite des nourrissons sont publiés dans Nature, impliquant notamment des équipes du laboratoire 2I (UVSQ/Inserm) et du laboratoire VIM (UVSQ/INRAE).
Cette étude met en lumière la description de drogues capables d’inhiber la multiplication du virus respiratoires syncytial en cellules et chez la souris en « solidifiant » les usines virales. Ces usines sont des organelles liquides, un mode de compartimentalisation cellulaire très courant et au cœur de nombreux processus biologiques. C’est la première fois qu’on décrit une drogue ciblant ces structures qui impacte un processus biologique en cellules et in vivo.
Résultats
Au sein d’une cellule, des compartiments permettent d’organiser les différentes activités, comme les mitochondries qui sont spécialisées dans la production d’énergie. Ces dernières années, de nombreux travaux ont montré l’importance dans l’organisation des activités cellulaires d’une nouvelle catégorie de compartiments : les organelles sans membrane aussi appelés organelles liquides ou biocondensats. Ces compartiments se forment par séparation de phase comme de l’huile formant des gouttelettes dans l’eau. Ils interviennent dans des processus physiologiques ou pathologiques aussi importants que variés comme le développement, l’immunité, l’activité neurologique, les processus dégénératifs ou tumoraux, etc.
Le virus respiratoire syncytial (RSV) est le principal agent de la bronchiolite du nourrisson, première cause d’hospitalisation des nourrissons en France. Il est aussi responsable d’infections très sévères voire mortelles chez les sujets âgés ou fragilisés. A ce jour il n’existe aucun vaccin ni antiviral curatif utilisable contre le RSV. Le RSV se multiplie au sein d’usines virales dans le cytoplasme des cellules infectées qui sont des organelles liquides formés par séparation de phase.
Dans ces travaux, l’équipe ATIP AVENIR décrit des composés chimiques capables de bloquer la multiplication du RSV en figeant ses usines virales. En présence du composé chimique, les usines virales perdent leur organisation et leur caractère liquide en quelques minutes. Ces usines « solidifiées » ne sont alors plus capables d’assurer la multiplication du virus bloquant ainsi sa réplication dans les cellules. Ces composés sont efficaces in vivo puisqu’ils inhibent la multiplication du RSV dans un modèle d’infection de la souris. La rapidité d’action de ces composés ciblant les usines virales en fait des candidats de choix pour le traitement d’infections aigues.
Perpectives
En conclusion, ces résultats démontrent que les organelles liquides peuvent être ciblés par des petites molécules qui altèrent leurs propriétés physiques et bloquent ainsi leur fonctionnement. La portée de cette découverte dépasse le traitement du RSV. En effet le contrôle des propriétés des organelles liquides par des drogues pourrait permettre de bloquer la multiplication d’autres virus tels que la rougeole, la rage ou Ebola ou encore de moduler des processus physio-pathologiques impliquant les organelles liquides tels que transformation cellulaire, réponse immunitaire, fonctionnement neuronal.
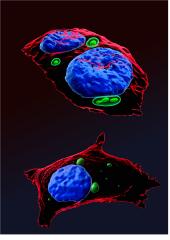
Légende
En haut : une cellule infectée par le RSV en l’absence de drogue. Le noyau est en bleu, la présence de 2 noyaux témoigne d’une fusion de 2 cellules formant un syncytia typique de l’infection par le RSV. Les contours cellulaires apparaissent en rouge. Les usines virales, en vert, sont liquides et contiennent des granules liquides.
En bas : une cellule infectée a été traitée par la drogue, les usines virales sont solides et les granules liquides ont disparu.
Images réalisées sur le microscope Leica SP8 de la plateforme Cymages et reconstruites avec le logiciel Imaris.
Résultats
Au sein d’une cellule, des compartiments permettent d’organiser les différentes activités, comme les mitochondries qui sont spécialisées dans la production d’énergie. Ces dernières années, de nombreux travaux ont montré l’importance dans l’organisation des activités cellulaires d’une nouvelle catégorie de compartiments : les organelles sans membrane aussi appelés organelles liquides ou biocondensats. Ces compartiments se forment par séparation de phase comme de l’huile formant des gouttelettes dans l’eau. Ils interviennent dans des processus physiologiques ou pathologiques aussi importants que variés comme le développement, l’immunité, l’activité neurologique, les processus dégénératifs ou tumoraux, etc.
Le virus respiratoire syncytial (RSV) est le principal agent de la bronchiolite du nourrisson, première cause d’hospitalisation des nourrissons en France. Il est aussi responsable d’infections très sévères voire mortelles chez les sujets âgés ou fragilisés. A ce jour il n’existe aucun vaccin ni antiviral curatif utilisable contre le RSV. Le RSV se multiplie au sein d’usines virales dans le cytoplasme des cellules infectées qui sont des organelles liquides formés par séparation de phase.
Dans ces travaux, l’équipe ATIP AVENIR décrit des composés chimiques capables de bloquer la multiplication du RSV en figeant ses usines virales. En présence du composé chimique, les usines virales perdent leur organisation et leur caractère liquide en quelques minutes. Ces usines « solidifiées » ne sont alors plus capables d’assurer la multiplication du virus bloquant ainsi sa réplication dans les cellules. Ces composés sont efficaces in vivo puisqu’ils inhibent la multiplication du RSV dans un modèle d’infection de la souris. La rapidité d’action de ces composés ciblant les usines virales en fait des candidats de choix pour le traitement d’infections aigues.
Perpectives
En conclusion, ces résultats démontrent que les organelles liquides peuvent être ciblés par des petites molécules qui altèrent leurs propriétés physiques et bloquent ainsi leur fonctionnement. La portée de cette découverte dépasse le traitement du RSV. En effet le contrôle des propriétés des organelles liquides par des drogues pourrait permettre de bloquer la multiplication d’autres virus tels que la rougeole, la rage ou Ebola ou encore de moduler des processus physio-pathologiques impliquant les organelles liquides tels que transformation cellulaire, réponse immunitaire, fonctionnement neuronal.

Légende
En haut : une cellule infectée par le RSV en l’absence de drogue. Le noyau est en bleu, la présence de 2 noyaux témoigne d’une fusion de 2 cellules formant un syncytia typique de l’infection par le RSV. Les contours cellulaires apparaissent en rouge. Les usines virales, en vert, sont liquides et contiennent des granules liquides.
En bas : une cellule infectée a été traitée par la drogue, les usines virales sont solides et les granules liquides ont disparu.
Images réalisées sur le microscope Leica SP8 de la plateforme Cymages et reconstruites avec le logiciel Imaris.
Informations complémentaires
En savoir plus
Lien vers la publication : https://rdcu.be/cnVx4
> Unité Infection et Inflammation (2I - UMR 1173 - UVSQ/Inserm)
Equipe ATIP AVENIR
> Laboratoire Virologie et Immunologie moléculaires (VIM - UMR 0892 UVSQ/INRAE)
Contact chercheur : marie-anne.rameix-welti@uvsq.fr
Premier auteur : Jennifer Risso-Ballester Post-doctorante ATIP AVENIR U1173
Co derniers et co-corresponding auteurs : Marie-Anne Rameix-Welti (Paris-Saclay UVSQ UMR 1173 et APHP Hopital Ambroise Paré) ; Ralf Altmeyer (Helmholtz International Lab for Anti-Infectives, State Key Laboratory of Microbial Technology, Microbial Technology Institute, Shandong University, 266237 Qingdao, P.R. China. ;Current affiliation: School of Public Health, University of Hong Kong, Hong Kong SAR, P.R. China.)
L’étude implique entre autres une équipe de l’INRAe de Jouy-en-Josas (VIM)
• Liste des auteurs de la publication
Authors: Jennifer Risso-Ballester1, Marie Galloux2, Jingjing Cao3, Ronan Le Goffic2, Fortune Hontonnou2, Aude Jobart-Malfait1, Aurore Desquesnes1, Svenja M. Sake4, Sibylle Haid4, Miaomiao Du3, Xiumei Zhang3, Huanyun Zhang3, Zhaoguo Wang5, Vincent Rincheval1, Youming Zhang3, Thomas Pietschmann4, Jean-François Eléouët2*, Marie-Anne Rameix-Welti1,6, £,*, Ralf Altmeyer3,7,£,*
Affiliations:
1 Université Paris-Saclay, INSERM, Université de Versailles St. Quentin, UMR 1173 (2I), Versailles, France.
2 Unité de Virologie et Immunologie Moléculaires (UR892), INRAE, Université Paris-Saclay, 78352 Jouy-en-Josas, France.
3 Helmholtz International Lab for Anti-Infectives, State Key Laboratory of Microbial Technology, Microbial Technology Institute, Shandong University, 266237 Qingdao, P.R. China.
4 Helmholtz International Lab for Anti-Infectives, Institute for Experimental Virology; Twincore - Centre for Experimental and Clinical Infection Research; a joint venture of Hannover Medical School (MHH) and Helmholtz Centre for Infection Research (HZI), Hannover, Germany.
5 Qingdao Municipal Center for Disease Control and Prevention, 266033 Qingdao, P.R. China.
6 Assistance Publique des Hôpitaux de Paris, Université Paris Saclay, Hôpital Ambroise Paré, Laboratoire de Microbiologie, Boulogne-Billancourt, France.
7 Current affiliation: School of Public Health, University of Hong Kong, Hong Kong SAR, P.R. China.
£ Equal contributors.
> Site Inserm
Lien vers la publication : https://rdcu.be/cnVx4
> Unité Infection et Inflammation (2I - UMR 1173 - UVSQ/Inserm)
Equipe ATIP AVENIR
> Laboratoire Virologie et Immunologie moléculaires (VIM - UMR 0892 UVSQ/INRAE)
Contact chercheur : marie-anne.rameix-welti@uvsq.fr
Premier auteur : Jennifer Risso-Ballester Post-doctorante ATIP AVENIR U1173
Co derniers et co-corresponding auteurs : Marie-Anne Rameix-Welti (Paris-Saclay UVSQ UMR 1173 et APHP Hopital Ambroise Paré) ; Ralf Altmeyer (Helmholtz International Lab for Anti-Infectives, State Key Laboratory of Microbial Technology, Microbial Technology Institute, Shandong University, 266237 Qingdao, P.R. China. ;Current affiliation: School of Public Health, University of Hong Kong, Hong Kong SAR, P.R. China.)
L’étude implique entre autres une équipe de l’INRAe de Jouy-en-Josas (VIM)
• Liste des auteurs de la publication
Authors: Jennifer Risso-Ballester1, Marie Galloux2, Jingjing Cao3, Ronan Le Goffic2, Fortune Hontonnou2, Aude Jobart-Malfait1, Aurore Desquesnes1, Svenja M. Sake4, Sibylle Haid4, Miaomiao Du3, Xiumei Zhang3, Huanyun Zhang3, Zhaoguo Wang5, Vincent Rincheval1, Youming Zhang3, Thomas Pietschmann4, Jean-François Eléouët2*, Marie-Anne Rameix-Welti1,6, £,*, Ralf Altmeyer3,7,£,*
Affiliations:
1 Université Paris-Saclay, INSERM, Université de Versailles St. Quentin, UMR 1173 (2I), Versailles, France.
2 Unité de Virologie et Immunologie Moléculaires (UR892), INRAE, Université Paris-Saclay, 78352 Jouy-en-Josas, France.
3 Helmholtz International Lab for Anti-Infectives, State Key Laboratory of Microbial Technology, Microbial Technology Institute, Shandong University, 266237 Qingdao, P.R. China.
4 Helmholtz International Lab for Anti-Infectives, Institute for Experimental Virology; Twincore - Centre for Experimental and Clinical Infection Research; a joint venture of Hannover Medical School (MHH) and Helmholtz Centre for Infection Research (HZI), Hannover, Germany.
5 Qingdao Municipal Center for Disease Control and Prevention, 266033 Qingdao, P.R. China.
6 Assistance Publique des Hôpitaux de Paris, Université Paris Saclay, Hôpital Ambroise Paré, Laboratoire de Microbiologie, Boulogne-Billancourt, France.
7 Current affiliation: School of Public Health, University of Hong Kong, Hong Kong SAR, P.R. China.
£ Equal contributors.
> Site Inserm









 Etudiants
Etudiants